
現代の健康産業において、カプセルのサプリメントは人々の日常生活の重要な一部となっている。ビタミンであれ、ミネラルであれ、ハーブエキスであれ、カプセルはその利便性、正確な服用量、保存のしやすさから支持されている。では、カプセルはどのように製造されているのでしょうか?この記事では、カプセルサプリメントの製造工程を包括的に分析します。 カプセルサプリメント, 原材料の選択から生産技術、品質管理、規制要件に至るまで。.
原材料の選択と配合設計
有効成分の選択と基準
有効成分には、ビタミン、ミネラル(例えば、Mg2+、Zn2+、および ハーブエキス (クルクミン、ジンセノサイドなど)。.
選考基準
- 高純度: 正確な投与と安定した有効性を確保するためには、中核となる活性物質の純度が99%($>99%$)以上でなければならない。.
- ソーシング認証: 有機認証や非遺伝子組み換え認証など、トレーサビリティのある認証原料を優先すること。これらの認証は、安全性、持続可能性、環境コンプライアンスを保証します。.
- 標準化されたエキス: ハーブ原料の場合、すべてのバッチで活性マーカー化合物の一貫した含有量を確保するために、標準化エキスを選択する必要があります。.
賦形剤(副原料)の選択
賦形剤は、形を整え、円滑な製造を確保し、バイオアベイラビリティを高めるために使用される。.
| 素材タイプ | 一般的な例 | 主要機能 | 比較 |
| フィラー | 微結晶セルロース(MCC)、乳糖 | 正確な充填のために錠剤/カプセルに容量を加えます。. | MCCは天然で不活性であり、優れた流動性を提供する。. |
| 潤滑油 | ステアリン酸マグネシウム | 粉体と機械の摩擦を減らし、生産効率を向上させる。. | 広く使用されているが、高用量は崩壊時間に影響する。. |
| カプセル・シェル | ゼラチン | 動物由来、低コスト、安定性良好。. | ベジタリアンには適さない。. |
| HPMCベジタリアン・シェル | 植物由来で、ベジタリアンや宗教上の制限に適している。. | コストがやや高く、湿気に弱い。. |
製剤開発と試験
投与量の計算: 臨床研究と推奨食事摂取量(RDA)または耐容上限摂取量(UL)に基づいて、有効成分の量を正確に決定する。.
互換性評価: 有効成分の分解を防ぐために、処方中のすべての原材料(活性剤および賦形剤)について、潜在的な化学反応や物理的相互作用を評価する。.
安定性試験:
- 加速老化試験: 完成した製品は、極端な条件下(例えば、高温40℃、高湿度75% RH)に置かれ、短期間での賞味期限を予測する。これにより、保存期間中、ラベルに記載された効能が少なくとも90%維持されます。.
サステナビリティとクリーンラベルの動向
現代の製剤は、持続可能性と「クリーンラベル」を重視している:
- 植物由来成分の使用: 動物由来成分の代わりに、植物エキスと植物性タンパク質を最大限に使用する。.
- 動物性コラーゲンへの依存度の低減: 内因性コラーゲン産生を促進する成分(例:ビタミンC、ビオチン)や、ベジタリアンや倫理的な消費者の要求に応えるためのビーガン代替品へのシフト。.
カプセル・サプリメントの製造工程
カプセルの製造工程では、厳格なGMP(適正製造基準)に従い、あらかじめ形成された殻に粉末や顆粒を充填する。.
原材料の準備と前処理
- 計量: すべての有効成分と賦形剤は、バッチ式に従って正確に計量される。.
- 粉砕とふるい分け: 原料を必要な細かさに粉砕し、ふるいに通して塊や不純物を取り除き、粒度分布を均一にする。.
🧪 ブレンディング
- ドライミキシング: 秤量・処理された粉末原料はすべて、専用のブレンダー(Vブレンダー、三次元ミキサーなど)で均一に混合されます。均質性を確保することは、すべてのカプセルに正確で一貫した投与量を確保するために非常に重要です。.
- 潤滑油の添加: 潤滑剤(ステアリン酸マグネシウムなど)は、効率的な充填に不可欠な粉末の流動性を高めるため、配合の最終段階で添加される。.
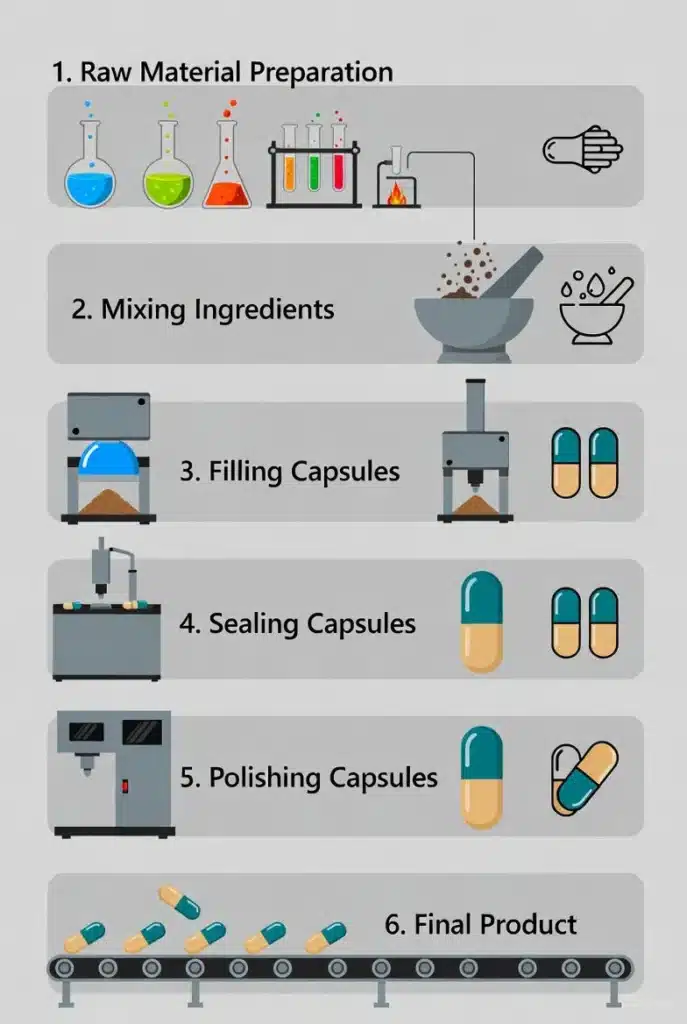
💊 カプセル化
- カプセル殻の分離: 自動または半自動カプセル充填機は、あらかじめ形成されたカプセルシェルを開封し、分離する。.
- パウダー充填: 均一にブレンドされた粉末は、カプセルシェルの下部ボディ(または容器)に充填される。.
- クロージングとロック: カプセルの上部(キャップ)は下部の本体に再び接合され、しっかりとロックされる。.
研磨と検査
- 研磨: カプセル研磨機でカプセル表面に残った粉を拭き取り、滑らかできれいな仕上がりにする。.
- 体重チェック 充填量の一貫性と正確さを確認するため、無作為のサンプルでカプセルの重量のばらつきをチェックする。.
- 金属探知: 最終製品は、消費者の安全性を確保するため、潜在的な金属汚染物質がないか検査される。.
📦 ポスト処理
- 一次梱包: 完成したカプセルは、製品を直接収容する容器(ボトル、ブリスターパックなど)に包装される。.
- 二次梱包: 一次梱包をカートンに入れ、最終ラベルを貼り、箱詰めして出荷する。.
- 完成品のテストとリリース: 物理化学的および微生物学的テストを含む最終品質管理チェックが行われる。バッチは、すべての品質仕様に完全に適合していることが確認された後、流通に供される。.
設備と施設の要件
高品質のサプリメント製造は、適正製造基準(GMP)ガイドラインに準拠した高度な設備と施設レイアウトに依存しています。.
I.中核生産設備リスト
次の表は、カプセルや錠剤の製造ラインに必要な設備の概要を、機能とコスト範囲に焦点を当ててまとめたものである。.
| 設備名 | コア機能 | 価格帯(人民元) |
| ブレンダー(V型、3Dミキサーなど) | 原料粉末の均一な混合を実現 | 20,000~150,000円 |
| カプセル充填機または高速錠剤機 | 製剤化(粉末充填または錠剤圧搾) | 10万円~50万円 |
| 乾燥装置(流動層乾燥機など) | 湿った顆粒を素早く均一に乾燥(湿式造粒用) | 8万円~30万円 |
| 自動包装機(ボトル/ブリスター) | 製品の最終包装、シールの完全性の確保 | 10万円~40万円 |
| 品質検査機器(X線スキャナーなど) | 製品の重量、硬度をチェックし、金属や汚染物質を検出する。 | 15万円~80万円 |
II.施設レイアウトと環境管理
施設はワークフローに従って科学的に仕切られ、二次汚染を防ぐために環境パラメータを厳密に管理しなければならない。.
- クリーンルームのゾーニング
- 原料エリア: 材料の受け入れ、検査、保管のための専用エリア。.
- 生産エリア(クリーンゾーン): 高い清浄度レベル(グレードDまたはCなど)を維持しなければならない中核的な製造エリア。.
- 梱包エリア: 完成品の最終密封、箱詰め、ラベル貼りのために指定された区域。.
- 空気ろ過システム: 効率的なHEPAフィルター(高効率微粒子エアフィルター)システムを導入して、製造エリアの空気清浄度を確保し、微粒子や微生物汚染を制御しなければならない。.
III.規模の選択と投資の推定
- スケールのオプション:
- 研究室のグレード: 手動または半自動装置を使用し、小バッチの配合試験や研究開発に適している。.
- 工業用グレード: 完全自動化された生産ラインを活用し、投資額は通常50万~200万人民元を超え、高生産能力と低単価を目標としている。.
- コスト見積もり:
- 小規模な生産ライン(基本的な設備と簡単なクリーンルームのセットアップを含む)のスタート資金は、およそ10万~50万人民元である。.
- 合理的な運用では、小規模回線の投資収益率(ROI)期間は一般に1~2年である。.
品質管理と規制遵守
厳格な品質管理(QC)と規制の包括的な遵守は、あらゆる健康補助食品ブランドの信頼性と市場での存続可能性の基盤である。.
I.エンド・ツー・エンドの品質管理(QC)
製品の安全性と有効性を確保するために、品質管理は製造の各段階に組み込まれなければならない。.
- イン・プロセス・モニタリング(IPM):
- 体重と投与量: カプセルや錠剤の平均重量と重量のばらつきをリアルタイムで監視し、投与精度を保証します。.
- 崩壊時間: 錠剤またはカプセル剤が特定の液体中で崩壊するのに要する時間のサンプル試験。これは通常、有効成分の放出を確実にするために30分未満であることが要求される。.
- バッチ・リリース・テスト:
- 微生物の限界: 大腸菌$、カビ、酵母の検査により、製品に微生物汚染がないことを確認する。.
- 重金属: 鉛(Pb)、ヒ素(As)、カドミウム(Cd)、水銀(Hg)の検査。レベルは国の安全基準値を十分に下回っていなければならない。.
- 溶解速度: 有効成分がヒトの消化器官内で予想される速度と範囲で溶解し、適切に吸収されるようにする。.

- イン・プロセス・モニタリング(IPM):
- 体重と投与量: カプセルや錠剤の平均重量と重量のばらつきをリアルタイムで監視し、投与精度を保証します。.
- 崩壊時間: 錠剤またはカプセル剤が特定の液体中で崩壊するのに要する時間のサンプル試験。これは通常、有効成分の放出を確実にするために30分未満であることが要求される。.
- バッチ・リリース・テスト:
- 微生物の限界: 大腸菌$、カビ、酵母の検査により、製品に微生物汚染がないことを確認する。.
- 重金属: 鉛(Pb)、ヒ素(As)、カドミウム(Cd)、水銀(Hg)の検査。レベルは国の安全基準値を十分に下回っていなければならない。.
- 溶解速度: 有効成分がヒトの消化器官内で予想される速度と範囲で溶解し、適切に吸収されるようにする。.
II.規制の枠組みと表示要件
ブランドは、主要なグローバル市場の規制の枠組みの中で事業を展開しなければならない。.
- 中国の規則 中国の健康食品製造に関する適正製造規範(GMP)を厳格に遵守し、製造、検査、記録管理に関する具体的な要件を定めている。.
- 国際基準: 米国FDA(食品医薬品局)のcGMP基準やEUのcGMP基準などの国際市場要件への準拠 リーチ 化学物質の登録、評価、認可および制限)。.
- ラベリング要件: ラベル情報は、真実かつ正確でなければならない:
- 成分リストと正確な投与量。.
- アレルゲンに関する警告(グルテン、大豆、ナッツ類など)。.
- 不適切な集団に対する健康強調表示と警告。.
III.一般的なリスクと対策
| リスク問題 | 根本原因 | 解決策/対策 |
| 微生物汚染 | 原材料のキャリーオーバー、クリーンルームの空気の質の低下 | 製造環境の定期的な紫外線消毒、従業員の厳格な衛生管理。. |
| 安定の失敗 | 湿気、光、熱により有効成分が劣化する。 | バリア性の高い包装材(アルミブリスターパックなど)、真空または窒素フラッシュ包装、温度/湿度管理された保管を使用する。. |
| 異物混入 | 機器の摩耗、外部汚染物質 | X線/金属検出器をインラインスキャンに使用する。. |
ケーススタディレッスン: 日本の小林製薬紅麹事件は、天然成分であっても、製造や保存が不適切であれば、有害な代謝産物(不注意に混入したシトリニンなど)を生成し、広範な健康問題や製品回収につながる可能性があることを浮き彫りにした。企業は、紅麹の毒物学的モニタリングを強化しなければならない。 原料 サプライチェーンと中間製品。.
IV.認証経路とブランドの信頼
認証は、市場で受け入れられ、消費者の信頼を得るための非常に効果的な方法である。.
- マネジメント基礎資格: ISO22000(食品安全マネジメントシステム)の認証を取得することで、体系的なリスクマネジメントの枠組みが確立される。.
- プレミアム・トラスト認定: 有機認証、コーシャ認証、ハラール認証を追求し、製品の差別化を図り、ブランドの信頼を大幅に高め、国際競争力を向上させる。.
課題、革新、そして将来の展望
I.主な課題
この業界は、当面のハードルにいくつか直面している:
- 原材料のボラティリティ: サプライチェーンの混乱 また、地政学的な不安定さによって、主要原材料の価格や入手が不安定になることも多い。.
- 環境圧力: 消費者の需要の高まりと規制の強化 プラスチック代替品 持続可能なパッケージング・ソリューションへの移行を義務付ける。.
- パーソナライズされた生産: の能力を拡大する必要がある。 オンデマンド・カスタマイズ・サプリメント 個々の遺伝的なニーズや食事上のニーズに対応するためである。.
II.イノベーションの原動力
テクノロジーとサイエンスが重要なイノベーションの原動力となっている:
- AIに最適化された処方: 人工知能(AI)を活用してデータを迅速に分析し、有効性と安定性を高めるために成分比率を最適化する。.
- ナノテクノロジー: ナノカプセル化技術を採用することで、敏感な活性化合物を保護し、吸収率とバイオアベイラビリティを大幅に向上させる。.
- 持続可能な素材: 従来のゼラチンやHPMCに代わるアルギン酸ベースのカプセルシェルなど、環境に優しい先進的な賦形剤やパッケージングの開発。.
III.今後の展望
- 2025年以降の市場展望: 完全自動化とリアルタイムのQC監視を特徴とするスマート・ファクトリーが、今後ますます市場を席巻していくだろう。.
- EコマースOEMの優位性: Eコマースの相手先ブランド製造(OEM)モデルは、迅速な製品立ち上げとスケーラブルな供給のための主要ルートとなり、グローバルな消費者直販のニーズに応える。.
結論
このプロジェクトは、健康補助食品分野での成功に不可欠な強固な基盤を概説するものです。優れた原料の調達、GMPに準拠した施設設計、包括的な品質管理など、厳格な要件を定義しました。準拠した高品質のカプセルを製造することは、単なる製造ステップではなく、健康産業の信頼と成長を支える基盤なのです。私たちは今、計画から実行に移す準備を整えています。.
生産プロセスの詳細を把握した次のステップは、それをより広いビジネスと規制の文脈の中に位置づけることである。私たちの コンセプトから市場投入までの包括的なガイダンスのために。.



